LA NOTIFICACIÓN POR SOSPECHAS DE REACCIONES ADVERSAS SE REDUCE NOTABLEMENTE EN 2023
La Aemps recibió 42.333 notificaciones durante el pasado año según el Informe Anual del Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano

La notificación de sospechas de reacciones adversas a medicamentos ha vuelto en 2023 a los niveles habituales en el periodo prepandémico según los datos dados a conocer este lunes por la Agencia Española de Medicamentos y Productos Sanitarios (Aemps), en el Informe Anual del Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano (SEFV-H), correspondiente al pasado año.
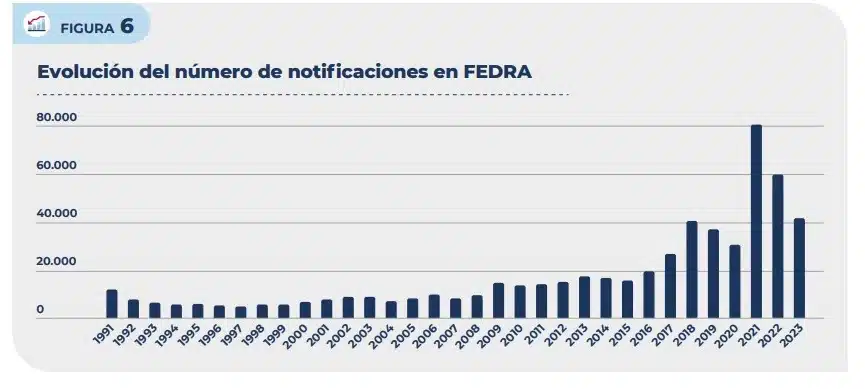
En 2023, se recibieron un total de 42.333 notificaciones de sospechas de reacciones adversas a medicamentos, una cifra que se mantiene en la línea de los registros previos a la llegada del Covid en 2018 y que marca una clara diferencia especialmente con respecto a los años 2021 y 2022 en los que las sospechas superaron las 80.000 y 60.000 notificaciones respectivamente.
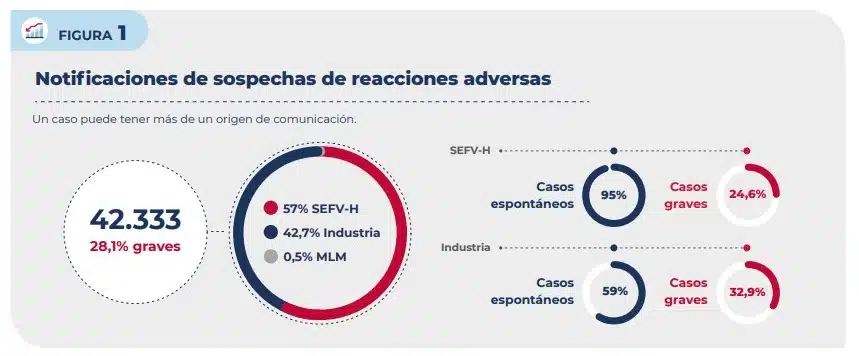
Según los datos del informe, a lo largo de 2023 se han registrado en FEDRA, la base de datos que registra las notificaciones, un total de 42.333 casos de sospechas de reacciones adversas a medicamentos o de acontecimientos adversos tras recibir una vacuna, de los cuales un 57% se notificaron directamente a los centros autonómicos de farmacovigilancia (SEFV-H), un 42,7% a través de la industria farmacéutica y un 0,5% procedentes de la revisión de la literatura científica (MLM, medical literature monitoring). Si bien la Aemps recuerda que un caso puede haber sido comunicado por más de una vía.
Del total de los casos notificados al SEFV-H, un 95% fueron notificaciones espontáneas. Para los casos notificados a través de la industria farmacéutica este porcentaje fue de un 59%. El resto de casos procedían de sistemas de recogida de información organizada, tales como estudios observacionales, programas de seguimiento de pacientes o acceso al medicamento a través del uso compasivo. Durante el año 2023 ha seguido teniendo un alto impacto la gestión de las notificaciones relacionadas con las vacunas Covid-19 recibidas.
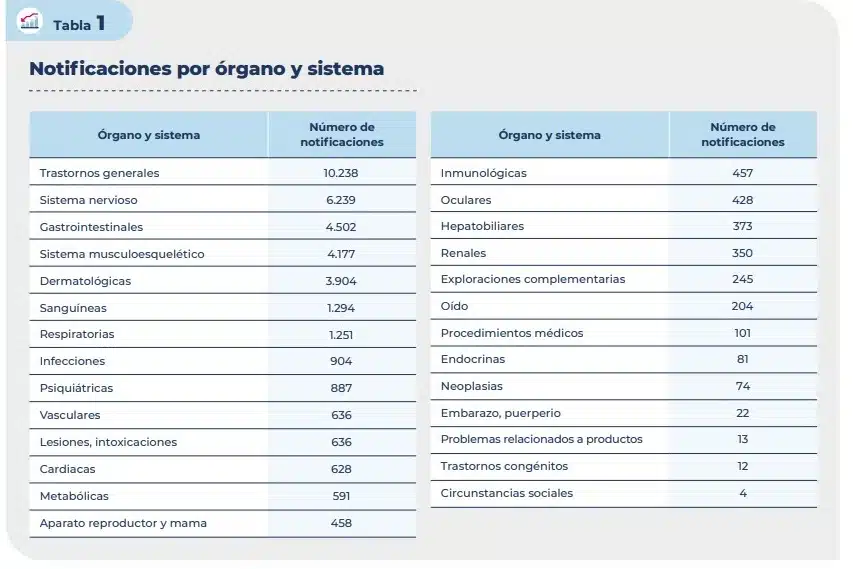
En cuanto a la gravedad, de los 42.333 casos recibidos, 11.899 (28,1%) fueron graves (mortal, ingresa o prolonga hospitalización, produce incapacidad, defecto congénito o médicamente relevante). Para los casos notificados al SEFV-H, el porcentaje de casos graves fue del 24,6%, mientras que para los casos notificados a través de la industria farmacéutica este porcentaje fue del 32,9%.
la mayor parte de las notificaciones recibidas por el SEFV-H las realizaron los profesionales sanitarios, en concreto, el 60,8% los profesionales médicos, el 19,9% los profesionales de enfermería y el 10,3% los profesionales farmacéuticos.
En relación con las notificaciones enviadas directamente al SEFV-H, y considerando los datos de población del Instituto Nacional de Estadística, se estima que se notifican 50 casos por cada 100.000 habitantes. De los datos de los casos notificados directamente al SEFV-H, un 8,3% de los 24.154 describían reacciones adversas desconocidas para el medicamento que se consideró sospechoso, tomando como referencia su ficha técnica.
Las notificaciones graves además de desconocidas fueron un 4,5%. El análisis de estos casos tiene gran valor para la generación de señales de farmacovigilancia, entendiendo como tal, potenciales nuevas reacciones adversas que deben seguir investigándose.
Con respecto a las características demográficas de los pacientes, la mayor parte de las notificaciones corresponden a pacientes adultos, seguido de mayores de 65 años. La edad generalmente está bien documentada, a diferencia de las notificaciones que se reciben a través de la industria farmacéutica, en las cuales se desconoce la edad del paciente en el 23,3% de los casos recibidos en 2023. Son más frecuentes las notificaciones que involucran al sexo femenino (66,4%).
40 años del SEFV-H
El SEFV-H, que celebra en 2024 su 40º aniversario, ha recogido durante estos años cerca de 600.000 casos de sospechas de reacciones adversas a medicamentos y acontecimientos adversos tras la vacunación, cuyo análisis ha originado numerosas señales de farmacovigilancia.
Fuente: Diario Farma
Volver